আরেক রকম ● ত্রয়োদশ বর্ষ একবিংশ সংখ্যা ● ১-১৬ নভেম্বর, ২০২৫ ● ১৬-৩০ কার্তিক, ১৪৩২
প্রবন্ধ
আত্মঘাতী ইমিউনিটির নিয়ন্ত্রণ ও মেডিসিনের নোবেল
স্বপন ভট্টাচার্য
শরীরের নাম মহাশয় হতে পারে কিন্তু এই মহাশয় যেই মুহূর্তে মাতৃজঠরের নিরাপদ আশ্রয় থেকে আলো-বাতাসের পৃথিবীতে অবতীর্ণ হন, সেই মুহূর্ত থেকে সম্মুখীন হন এক সম্পূর্ণ নতুন বৈরী জগতের যেটির অধিবাসীরা আবার প্রধানত অদৃশ্য এবং যারা তাদের তূণীরে থাকা যে কোনও বাণেই তাঁকে পেড়ে ফেলতে সক্ষম। ব্যাকটেরিয়া, ভাইরাস, ছত্রাক, এককোষী আদ্যপ্রাণী, হাজার এক বিপজ্জনক বিজাতীয় বস্তু - যারা এই জগতের অধিবাসী, তাদের সঙ্গে প্রতিনিয়ত যুঝে এই মহাপ্রাণটিকে যাকে বলে ধুক ধুক করে বাঁচিয়ে রাখার হ্যাপা কম নয়, কেননা তারা সংখ্যায় এবং বৈচিত্রে অগনন।
এত রকমের শত্রুর মোকাবিলা করার জন্য প্রকৃতি প্রাণীকূলকে যে শস্ত্রসম্ভার দিয়েছে সেটিও বিপুলায়তন এবং একটি সুস্থ শিশু প্রকৃতিদত্ত এইসব অস্ত্রশস্ত্র নিয়েই জন্মায় বলেই অন্তিমের শ্বাস পর্যন্ত এই প্রতিরক্ষা ব্যবস্থা শত্রুদের সামনে অসম্ভব শক্তিশালী এক ব্যারিকেড তৈরি রাখে। ব্যবস্থাটিকে আমরা অনাক্রম্যতা বা ইমিউনিটি বলে জানি এবং কেবলমাত্র জন্মগত উপাদানের উপর ছেড়ে না রেখে বাইরে থেকে বিশেষ বিশেষ উপাদান (যেমন ভ্যাকসিন) প্রয়োগে সেই ব্যবস্থাকে শানিয়ে তোলার কায়দাও আমাদের আয়ত্বে এসেছে।
তবে কিনা সিস্টেমটা বিশেষ বিশেষ ক্ষেত্রে এতটাই প্রতিক্রিয়াশীল শ্রেণিশত্রুর মতো কাজ করে বসে যে নিজের শরীরের উপাদানকেই ধংসের কাজে লিপ্ত হয়। এমনটা যে হয়, অর্থাৎ শরীরের তথাকথিত রোবাস্ট ইমিউন সিস্টেম যে সেই শরীরেরই প্রধানতম বৈরীভাবাপন্ন শত্রু হয়ে ওঠে, তা চিকিৎসকরা ঊনবিংশ শতাব্দীর গোড়া থেকেই অনুমান করতে পেরেছিলেন। ১৯০৮ সালে নোবেল প্রাইজ বিজয়ী চিকিৎসাবিজ্ঞানের এক মহাগুরু পল আর্লিচ (Paul Ehrlich) এই ঘটনাকে সনাক্ত করেছিলেন আতঙ্ক জাগানো এক শব্দবন্ধে - 'হরর অটোটক্সিকাস'। বাইরের আক্রমণ নাহয় সামাল দেবার জন্য ইমিউন সিস্টেম আছে, কিন্তু ভেতর থেকেই যে আক্রমণ তা সামাল দেয় কে? কীভাবে ইমিউন সিস্টেমের উপাদানসমূহকে আত্মঘাতী হয়ে ওঠার সম্ভাবনা থেকে রুখে দেয় শরীর তা আধুনিক চিকিৎসাবিজ্ঞানের তথা ইমিউনিটি সংক্রান্ত গবেষণার এক অতি জীবন্ত পরিসর। ২০২৫ সালের চিকিৎসাবিজ্ঞান-শারীরতত্ত্বের নোবেল প্রাইজ পেয়েছেন যৌথভাবে তিনজন এই বিশেষ ক্ষেত্রটিতে আলোকপাত করে। এঁরা হলেন মেরি ব্রাঙ্কো, ফ্রেড র্যামসডেল এবং শিমোন সাকাগুচি (Mary E. Brunkow, Fred Ramsdell and Shimon Sakaguchi)।

চিত্র-১: মেডিসিন ও শারীরতত্ত্বের বিভাগে ২০২৫ সালের নোবেল পুরস্কার বিজয়ীরা। (বাম দিক থেকে) মেরি ব্রান্কো, ফ্রেড র্যামসডেল ও শিমোন সাকাগুচি।
কোষনির্ভর ইমিউনিটির নিয়ন্ত্রণ নিয়ে পরীক্ষালব্ধ কিছু মোক্ষম প্রমাণ দাখিল করে তাঁরা দেখাতে পেরেছেন যে আমাদের বেঁচেবর্তে থাকার জন্য 'ইমিউন টলারেন্স' বা অনাক্রমন্যতা সহনশীলতাও সমান গুরুত্বপূর্ণ এবং তা অর্জন করার জন্য কিছু নিয়োজিত কোষবিশেষ এবং কিছু প্রোটিনের কার্যকারিতা একান্তই আবশ্যক বলে অনুমান। শুধু অটোইমিউন ডিজঅর্ডার নয়, ক্যান্সার চিকিৎসাতেও এদের ভূমিকা গুরুত্বপূর্ণ বিবেচিত হবার সুযোগ রয়েছে। আর্লিচের 'হরর' অতিমাত্রায় জীবন্ত উপপাদ্যই বটে! তবে তার আগে কিছু খুঁটিনাটি জেনে নিলে বোঝাটা সহজ হতে পারে অনুমান করি।
দ্বিবিধ অনাক্রম্যতা- জন্মগত এবং অভিজ্ঞতালব্ধ
ওই যে বলছিলাম, শরীরের প্রতিরক্ষা ব্যবস্থাটি একদম জন্মের মুহূর্ত থেকেই কাজে নেমে পড়ে, সেটা কীভাবে? আমাদের ত্বক, চোখের জল, নাকের জল, ঘর্মগ্রন্থি, অন্দরের অঙ্গ-প্রত্যঙ্গগুলোর গায়ের পিচ্ছল লাইনিং- যার নাম মিউকাস মেমব্রেন, কিছু বিশেষ বিশেষ প্রোটিন, শ্বাসনালীর রোমশ লাইনিং, অঙ্গবিশেষের অ্যাসিডিক সিক্রিশন - এগুলো সব আমরা নিয়েই জন্মাই এবং এরাই হল 'ফার্স্ট লাইন অফ ডিফেন্স' যা পরিবেশের বৈরিতার সঙ্গে গোড়া থেকেই যোঝে এবং শত্রুর বাছবিচার না করেই যোঝে। ইমিউনিটির এই প্রথম শাখাটিকে বলে ইনেট ইমিউনিটি (Innate Immunity), সহজ করে বললে জন্মগত ইমিউনিটি। দ্বিতীয় শাখাটির নাম অ্যাডাপ্টিভ ইমিউনিটি (Adaptive Immunity), আমরা যাকে অভিজ্ঞতালব্ধ অনাক্রম্যতা বলেছি এই অংশের শিরোনামে (চিত্র-২)। এটি কিন্তু বিশেষ এই অর্থে যে বাছবিচার তাকে করতেই হয়। জন্মগত প্রতিরক্ষার বাধা পেরিয়ে যখন কোনও জীবাণু শরীরে ঢুকে পড়ে এদের কাজ শুরু হয় তখন। এদের মানে কাদের? মুখ্যত তিন রকম উপাদানের উপর নির্ভর করে এই অভিজ্ঞতালব্ধ ইমিউনিটির কার্যকারিতা, এরা হল বি-কোষ, টি-কোষ এবং অ্যান্টিবডি। তিনটেই রক্তের উপাদান, বি এবং টি কোষ বলতে আসলে বলা হচ্ছে রক্তকোষ বি এবং টি লিম্ফোসাইটের কথা আর অ্যান্টিবডি হল রক্তরসের অংশ। কোনও বিশেষ জীবাণুর বিরুদ্ধে কার্যকরী প্রতিরক্ষা প্রদান করতে গেলে এদের প্রথমে সেই জীবাণুটিকে 'চিনতে' হয়। এটাই পূর্বশর্ত এবং চেনাশোনার ব্যাপারটা যেহেতু সময়সাপেক্ষ সেহেতু জন্মগত প্রতিরক্ষার মতো এই অভিজ্ঞতালব্ধ ইমিউন সিস্টেমের প্রাথমিক প্রতিক্রিয়া তাৎক্ষণিক নয়, বরং সময়সাপেক্ষ। কিন্তু এই শাখার একটি বিশেষ বৈশিষ্ট্য আছে, তা হল 'স্মৃতি'। একবার এনকাউন্টার সম্পন্ন হলে এরা শত্রুকে চিনে রাখে এবং সেটি দ্বারা পরবর্তী যে কোনও আক্রমণে দ্রুততর প্রতিক্রিয়া দেখিয়ে প্রতিরোধ করে।
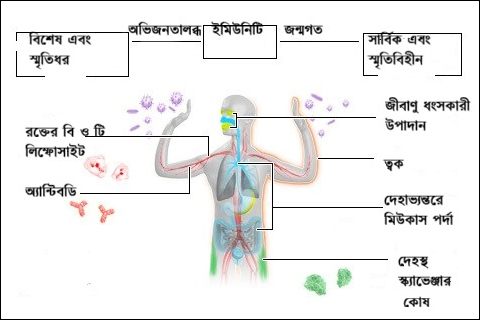
চিত্র-২: জন্মগত ও অভিজ্ঞতালব্ধ ইমিউনিটির পার্থক্য।
এই যে জীবাণুসমুহের মহাসমুদ্র, তাদের মধ্যে বিপুল সংখ্যককে প্রতিরোধ করা এবং স্মৃতিতে রাখা - এ যে কী ভাবে সম্ভব হতে পারে তা দীর্ঘদিন ধরেই বিজ্ঞানীদের কাছে এক রহস্য ছিল। এখন আমরা জানি বি ও টি কোষ কোনও বাইরের এজেন্টকে প্রথম দফায় শত্রুপক্ষ অনুমানে চেনে এবং চেনে অ্যান্টিজেন রূপে। এই চেনাচেনির কাজটা সম্পন্ন হয় ওই বি ও টি কোষস্থিত সুনির্দিষ্ট গ্রাহক বা রিসেপটরের মাধ্যমে। এদের বলে যথাক্রমে বি সেল রিসেপ্টর (BCR) ও টি সেল রিসেপটর (TCR)। কার্যত এই সম্পর্ক তালা ও চাবির মতো বলা যায়, যেখানে একটি নির্দিষ্ট অ্যান্টিজেনের জন্য একটিই রিসেপটর। কিন্তু প্রতিটি ফরেন এজেন্টকে আলাদা আলাদাভাবে বাগে আনতে ঠিক যে কত সংখ্যক রিসেপটর তৈরির ক্ষমতা ওদের থাকতে হবে তা কল্পনাও করা যায় না, যেহেতু দৃশ্য-অদৃশ্য, আবিষ্কৃত-অনাবিষ্কৃত মিলে এমন সম্ভাব্য অ্যান্টিজেনের সংখ্যা অনুমানের অতীত! মানুষের কোষে থাকা ডিএনএ জিনিসটাকে এমন প্রতিটির জন্য আলাদা আলাদা জীন বহন করতে হলে স্রেফ জায়গায় কুলোবে না, কার্যত অসম্ভব সেটা। কোন বিচিত্র উপায়ে এই কাজটি হয় তার সমাধানে জাপানের বৈজ্ঞানিক সুসুমু টোনেগাওয়া (১৯৮৭ নোবেল প্রাইজ বিজয়ী) দেখালেন মানুষের জীনোমের একটা ছোট অংশই বিভিন্ন কম্বিনেশনের রিসেপটর তৈরি করতে পারে প্রয়োজনমাফিক এবং তাদের সংখ্যা একের পরে পনেরোটা শূন্য লাগালে যা দাঁড়ায়, তা হওয়া সম্ভব।
অনভিজ্ঞ বি লিম্ফোসাইটের (ইংরেজি নামটা সুন্দর - নাইভ) অ্যান্টিজেন চেনার কাজটি সম্পন্ন হলে সেটি অর্জিত অভিজ্ঞতার নিরিখে তালা খোলার চাবিটির হদিশ পেয়ে নির্দিষ্ট অ্যান্টিজেনের বিরুদ্ধে নির্দিষ্ট চাবি অর্থাৎ অ্যান্টিবডি উৎপাদনের কাজে নিয়োজিত হয়, এদের বলে প্লাজমা কোষ। অল্প কিছু কোষ রূপান্তরিত হয় মেমোরি সেল বা স্মৃতি কোষে এবং একই অ্যান্টিজেনের পরবর্তীকালের যে কোনও এনকাউন্টারে তার প্রতিক্রিয়া হয় তাৎক্ষণিক, প্রথমবারের মতো অত সময় লাগে না। বি-কোষের এই পরিণতিপ্রাপ্তির ব্যাপারটা ঘটে বোন ম্যারো বা অস্থিমজ্জায়। টি-কোষেরও একই নিয়মে অভিজ্ঞতা ও পরিণতির ব্যাপার রয়েছে এবং সেটা ঘটে থাইমাস নামক প্রত্যঙ্গে। টি-লিম্ফোসাইটের নাম টি-কোষ হওয়ার কারণটি অনুমান করা কঠিন নয়, ওই থাইমাস অঙ্গটি হল টি-কোষের পাঠশালা। এদের দুটি প্রকারভেদ আছে। একদল হল টি-হেল্পার কোষ (TH), বি ও টি লিম্ফোসাইটের সক্রিয় হয়ে ওঠা এবং অ্যান্টিবডি উৎপাদনে এদের আবশ্যিকভাবে সহায়ক ভূমিকা রয়েছে। অপর দলটি হল টি-কিলার বা ঘাতক কোষ (সাইটোটক্সিক টি লিম্ফোসাইট - CTL) যারা সরাসরি সংক্রামিত দেহকোষকে এবং টিউমার কোষকে ধ্বংস করে দেয় (চিত্র-২)। উভয়ের কাজের তফাৎ তো রয়েইছে, কোষগাত্রে থাকা প্রোটিনবিশেষের মধ্যেও তফাৎ রয়েছে। TH-কে চেনা যায় CD4 নামক একটা বিশেষ প্রোটিনের উপস্থিতি দিয়ে এবং CTL-কে চেনা যায় CD8 নামের অন্য আর একটা প্রোটিনের উপস্থিতি দিয়ে। এই কারণে এদের অন্যভাবে যথাক্রমে CD4+ এবং CD8+ কোষ নামে পরিচিতি দেবারও রীতি রয়েছে।
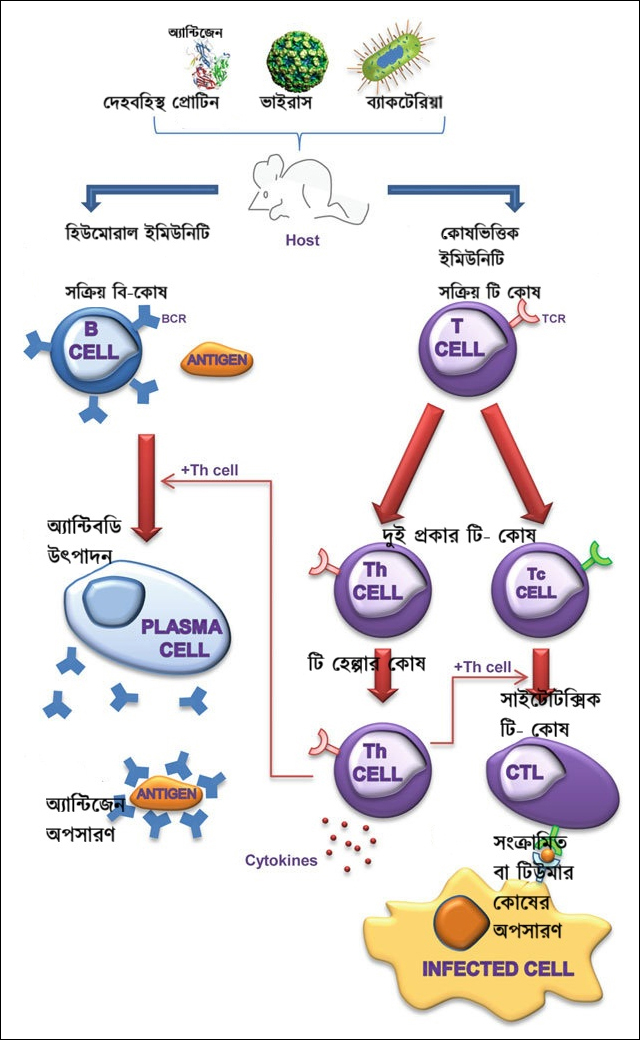
চিত্র-৩: কোষনির্ভর ইমিউনিটির দুটো শাখা - একটা হল হিউমোরাল ইমিউনিটি যা বি-কোষ দ্বারা পরিচালিত এবং অ্যান্টিবডি উৎপাদনের মাধ্যমে কাজটা করে তারা। দ্বিতীয় শাখাটি হল কোষভিত্তিক ইমিউনিটি যা টি-কোষ দ্বারা পরিচালিত। দু'রকম টি-কোষ আছে, টি-হেল্পার এবং ঘাতক বা সাইটোটক্সিক টি-কোষ। টি-হেল্পার কোষ অ্যান্টিবডি উৎপাদনে যেমন তেমনই ঘাতক টি-কোষের কাজেও সহায়তা করে।
সুতরাং দেখা যাচ্ছে বিপুল বৈচিত্রসম্পন্ন বি ও টি সেল রিসেপটর, অ্যান্টিবডি উৎপাদনে কোষগুলির ভূমিকা, তাদের স্মৃতিধারক ভূমিকা এবং শরীরে টিউমারের মতো অনভিপ্রেত কোষগুলোকে বাড়তে না দেওয়া - এগুলোই হল সহজ কথায় আমাদের ভালো থাকার, জীবাণুঘটিত রোগ-বালাই বাঁচিয়ে সুস্থ থাকার উপায়। কিন্তু এই সুস্থতার বিনিময়ে কিছু মূল্য শরীরকেও দিতে হতে পারে, কারণ যে রিসেপটরগুলি এই শস্ত্রসম্ভারের প্রধান আয়ূধ, তা কখনো কখনো যে দেহে তার সৃষ্টি, সে দেহেরই কোনও কোষকে ভুল করে 'ফরেন' ভেবে বসে এবং ধ্বংসে লিপ্ত হয়। এই ঘটনাই হল পল আর্লিচের 'হরর'! প্রশ্ন হল এর পরেও ইমিউন সিস্টেমটাকে শরীর সহ্য করে কী ভাবে? ইমিউনিটি সংক্রান্ত গবেষণার গোড়া থেকেই এই 'ইমিউন টলারেন্স' সংক্রান্ত আবিষ্কার নতুন নতুন বিস্ময়ের জন্ম দিয়েছে। এবারের নোবেল জয়ী গবেষণাও তার ব্যতিক্রম নয়।
শরীর যখন নিজেই নিজের শত্রু
শরীরের নাম মহাশয় হতে পারে, তবে যা সওয়াবে তাই সইবার ক্ষমতা তার সত্যিই নেই, এমন কি মহাশয়কে বাঁচিয়ে রাখার জন্য রক্তাশ্রিত যে বিপুল আয়োজন, তাকেই প্রতিনিয়ত বৈরী হয়ে ওঠার সম্ভাবনা থেকে দূরে রাখতে হয়, নয়তো বিপদ যে কত আর কত তার রকমফের, তা বলে শেষ করা যাবে না। অটো-ইমিউন ডিজঅর্ডারকে স্নায়ু বিকলন থেকে মস্তিষ্ক বিকলন পর্যন্ত নানা বৈকল্যের জন্য দায়ী করা যায় এমন প্রামাণ্য প্রতিপাদ্য প্রতিদিন জার্নালগুলিতে প্রকাশিত হচ্ছে। বোঝা যাচ্ছে, সুস্থ মানুষের দেহে এমন মিরজাফরী আক্রমণ প্রতিরোধের বা বাইপাস করার কিছু উপায় নিশ্চয়ই রয়েছে, নয়তো কোনও মানুষেরই যৌবনে উপনীত হওয়ার কথা নয়, তার আগেই নিজের ঘায়ে তার রোগজর্জর হয়ে মারা যাবার কথা। জাক মিলার (Jacques Miller) ১৯৬১ সালে সদ্যোজাত ইঁদুরের থাইমাস নামক প্রত্যঙ্গটি অপারেশন করে বাদ দিয়ে দেখেন সেটির ইমিউনিটি ব্যাপকভাবে হ্রাসপ্রাপ্ত এবং রক্তে একধরনের লিম্ফোসাইটও অনুপস্থিত। টি-কোষের উপস্থিতির এবং ইমিউনিটি প্রদানে তার গুরুত্ব প্রমাণে সেটাই প্রথম উল্লেখযোগ্য গবেষণা। এর বেশ কিছুদিন পরে প্রমাণ পাওয়া যায় (Philippa Marrack and John W. Kappler, 1987) যে টি-কোষ যারা থাইমাসে পুষ্ট হয়, তাদের মধ্যে কিছু অবশ্যই সেলফ-রিঅ্যাক্টিভ অর্থাৎ প্রকৃষ্ট ঘরশত্রু, কিন্তু থাইমাসে বেড়ে ওঠার পথে তাদের বেছে ছেঁটে ফেলার একটা ব্যবস্থা আছে, এই ধরণের ছেঁটে ফেলার পদ্ধতিকে বিজ্ঞানের ভাষায় বলে 'নেগেটিভ সিলেকশন'। এই ব্যবস্থাকে ইমিউন সিস্টেমের 'কেন্দ্রীয় সহনশীলতা' বা সেন্ট্রাল টলারেন্স বলা হয়ে থাকে। তবে এটাই যদি নিয়ম হয় তাহলে থাইমাসে বেছে বেছে ছেঁটে বাদ দেবার পরেও শরীর ওই সেলফ-রিঅ্যাক্টিভদের কবলে পড়ে কেন? অনুমান তখন থেকেই দৃঢ় হচ্ছিল যে এত কিছুর পরেও রক্তে যদি ঢুকেই পড়ে ওই ঘরশত্রুরা তাহলে তাদের নিকেশ করবার অন্য বিকল্প বা অতিরিক্ত উপায় নিশ্চয়ই আছে।
শিমোন সাকাগুচি ও অটোইমিউন রোগের কবলে পড়া ইঁদুর
কিয়োতো ইউনিভার্সিটিতে ডাক্তারির ডিগ্রি অর্জন করার পর শিমোন সাকাগুচির গবেষণার ক্ষেত্র হয়ে দাঁড়ালো এই 'সেন্ট্রাল টলারেন্স'। আইচি ক্যান্সার রিসার্চ সেন্টারে ড. নিশিজুকার ল্যাবে যোগ দিয়ে প্রথম যে উল্লেখযোগ্য রিপোর্টটি করেছিলেন তা হল, থাইমাস বাদ দেওয়া ইঁদুরের অটোইমিউন ডিজঅর্ডার সুস্থ ইঁদুর থেকে সুনির্দিষ্ট কিছু টি-কোষ আহরণ করে ইঞ্জেকশন দিলেই সারিয়ে তোলা সম্ভব। এই সুনির্দিষ্ট কোষগুলি যে CD4+ হেল্পার টি-কোষ তাতে কোনও সন্দেহ ছিল না কিন্তু সব হেল্পার বা CD4+ টি-কোষ যে তা পারে না সেটাও প্রমাণিত। সুতরাং অন্য কোন বৈশিষ্ট্য এদের মধ্যে আছে তা খুঁজতে থাকলেন তিনি। দেখলেন হেল্পার টি-কোষগুলোর মধ্যে একটা ছোট অংশ CD4-এর পাশাপাশি CD25 নামের অন্য একটি প্রোটিনও তৈরি করে। থাইমাস অপসারিত ইঁদুরের দেহে যদি সুস্থ ইঁদুরের দেহ থেকে CD4+ কোষসংগ্রহ করে CD25 প্রোটিনটা বাদ দিয়ে পুনরায় ইনজেক্ট করা হয় তাহলে সেই সুস্থ ইঁদুর ভয়াবহ আর্থাইটিস, প্যানক্রিয়াটাইটিস, থাইরয়েডাইটিস, গ্যাসট্রাইটিস সহ বিভিন্ন অটোইমিউন ডিজঅর্ডারের কবলে পড়ে। কিন্তু CD4+ CD25+ TH কোষ দ্বারা এই পরিস্থিতি আমূল বদলে দেওয়া যায় এবং ইঁদুর সেরে ওঠে। ইঁদুরের ইমিউন সিস্টেম মুখ্যত মানুষের মতোই, ফলে এই দিকনির্ণায়ক পরীক্ষার সাহায্যে শিমোন সাকাগুচি প্রমাণ করে দিলেন যে অটোইমিউন ডিজঅর্ডার নিয়ন্ত্রণে CD4+ CD25+ টি-কোষের অবিসংবাদিত ভূমিকা রয়েছে। 'রেগুলেটরি টি-সেল' বা নিয়ন্ত্রক টি- কোষ কথাটা তখনও পর্যন্ত কেউ কেউ স্রেফ অনুমানের বশবর্তী হয়ে ব্যবহার করতেন। সাকাগুচির এই পরীক্ষার ফলে সকলে মেনে নিলেন ইমিউন টলারেন্স নিয়ন্ত্রিত হয় টি-কোষের একটি উপশাখা বা সাবসেট দ্বারা যাদের রেগুলেটরি টি-কোষ বা সংক্ষেপে Treg বলে সনাক্ত করা যায় (চিত্র-৪)।
ম্যানহাটন প্রজেক্টের ইঁদুর ও ঘাতক ইমিউন সিস্টেম
টেনেসির 'ওক রিজ ন্যাশানাল ল্যাবোরেটরি ফর এ্যাটমিক এনার্জি' হিরোসিমায় ঘটনাটা ঘটানোর আগে প্রাণীকূলের ওপর সেই ঘটনার প্রতিক্রিয়া সম্পর্কে ভালো রকম ওয়াকিবহাল ছিল বলেই জানত যে ১৯৪০ সালেই তাদের ল্যাবে এ্যাটমিক বিকিরণের ফলে স্বাভাবিক ইঁদুরের চামড়া থেকে শুরু করে সব অঙ্গ-প্রত্যঙ্গেই ব্যাপক বৈকল্য দেখা দিয়েছে (চিত্র-৩)। এরা মারক প্রকৃতির অটোইমিউন ডিজঅর্ডারের শিকার এবং এদের নাম দেওয়া হয়েছে স্ক্রাফি (Scruffy mice) ইঁদুর।

চিত্র-৪: স্ক্রাফি ইঁদুর। এদের X-ক্রোমোজোমে একটি মিউটেশন এই ভয়ংকর অটোইমিউনিটির জন্য দায়ী।
এটা একটা মিউটেশনের ফল এবং মিউটেশন যখন পুং-প্রাণীতে তখনই কেবল স্ক্রাফির দেখা মিলছে, স্ত্রী-প্রাণী কিন্তু বেঁচে যাচ্ছে। আসলে স্ত্রী-প্রাণীতে তো দুটো X-ক্রোমোজোম, তার একটায় মিউটেশন থাকলেও অন্যটা স্বাভাবিক, কিন্তু পুং-প্রাণীর একটাই X-ক্রোমোজোম, আর কেউ সামাল দেবার সুযোগ নেই। এর থেকে সিদ্ধান্তে আসা গেল যে মিউটেশনটি রয়েছে X-ক্রোমোজোমে। স্ক্রাফির ধরন-ধারণ জানাছিল ঠিকই কিন্তু বহুদিন পর্যন্ত এটির জন্য যথার্থ কোনও জীনকে চিহ্নিত করা সম্ভব হয় নি।
মেরি ব্রান্কো এবং ফ্রেড র্যামসডেল কাজ করছিলেন ওকলাহোমার 'সেলটেক কায়রোসায়ন্সেস' নামের এক বায়োটেকনোলজি ল্যাবে। তাঁদের নজর পড়ল সেদিকে। নেহাতই 'কিউরিওসিটি ড্রিভেন প্রজেক্ট' - কিন্তু বিজ্ঞানে ওই কিউরিওসিটির মূল্যই সবচেয়ে বেশি! রেগুলেটরি টি-কোষ নিয়ে তখন অনেকেই কাজ করছেন কিন্তু প্রাণী মডেলে তা করবার তাগিদে ১৯৪০-এর স্ক্রাফিতে ফিরে যাওয়া ছিল এই গবেষক দুজনের মাস্টারস্ট্রোক। তাঁরা স্ক্রাফি ইঁদুরের X-ক্রোমোজোমের একটা ছোট অংশে ২০টি এমন জীন সনাক্ত করলেন যারা এই বিকলনের জন্য দায়ী হলেও হতে পারে। পরীক্ষার উপায় কি? উপায় স্বাভাবিক ইঁদুরের ওই একই জীনগুলোর সঙ্গে মিলিয়ে দেখা। সব কয়টি জীনে ব্যর্থ হবার পর শেষতমটিকে বাতিল করার মুখে খুঁজে পান একটিমাত্র ছোট্ট ত্রুটি যার দরুন একটা স্বাভাবিক প্রোটিন পুরোপুরি তৈরি হয়ে ওঠার আগেই অনাকাঙ্ক্ষিত ছেদ পড়ে যায়। প্রোটিনের রাসায়নিক গঠন কাঁটা-চামচের মাথার মতো, তাই নাম দেওয়া হল Forkhead Box P3 প্রোটিন এবং জীনটিকে চিহ্নিত করা হল Foxp3 নামে। কিন্তু এখানেই থামলেন না তাঁরা। এর পরে তাঁরা দেখালেন যে জীন স্থানান্তরণ করে যদি ওই স্ক্রাফি ইঁদুরে মিউটেশন হয়নি এমন Foxp3 জীন ঢুকিয়ে দেওয়া যায় তাহলে ঘটনা উলটে দেওয়া যায়, পরিষ্কার রেসকিউ অপারেশন, যার জন্য স্বাভাবিক Foxp3 প্রোটিন উৎপাদন দরকার। এর পরে ইঁদুর থেকে তাঁরা চলে এলেন মানুষে। মানুষের দুটো বংশানুক্রমিক রোগ IPEX (immune dysregulation, polyendocrinopathy, enteropathy, X-linked) syndrome or XLAAD (X-linked autoimmunity-allergic dysregulation) হল আদর্শ অটোইমিউন ডিজঅর্ডারের উদাহরণ। দুটোই বাচ্চা ছেলেদের মারক রোগ এবং কেবলমাত্র স্টেম সেল প্রতিস্থাপনেই তাদের বাঁচানো যায়। ওঁরা দেখালেন যে মানুষের X-ক্রোমোজোমে Foxp3-এর একটা সমরূপ আছে (Foxp3) এবং সেটার মিউটেশন বংশানুক্রমিকভাবে এই রোগগুলির জন্য দায়ী।
দু'য়ে মিলে বিস্ময়
আলাদা আলাদা ভাবে এই দুই আবিষ্কার, সাকাগুচির CD4+ CD25+ Treg কোষ এবং ব্রান্কো ও র্যামসডেলের Foxp3, এদের মধ্যে যে কোনও একটা যোগসূত্র আছে তা সাকাগুচি অনুমান করেছিলেন এবং সঙ্গে সঙ্গেই দেখালেন যে স্ক্রাফি ইঁদুরের রক্তে Treg নেই। তাছাড়াও সাকাগুচি ও ব্রান্কোরা দেখালেন যে Foxp3 প্রোটিনের উপস্থিতিতে স্বাভাবিক টি-হেল্পার কোষ (CD4+ কোষ) Treg কোষে পরিণত হয় (চিত্র-৪)। দুইয়ের এই যোগসূত্র গবেষণার নানা দিক খুলে দিল বিশ্বের বিভিন্ন প্রান্তেই। হাওয়ার্ড মেডিক্যাল স্কুলের আলেকজান্ডার রুডেন্সকির গ্রুপ দেখালেন যে থাইমাসে Foxp3 প্রোটিন যদি পৌঁছতেই না দেওয়া হয় তাহলে ইঁদুরের যে সমস্ত অটোইমিউন ডিজঅর্ডার দেখা যায় তার সঙ্গে স্ক্রাফি লক্ষণগুলোর খুব বেশি মিল রয়েছে। শুধু তাই নয়, তাদের Treg কার্যকারিতাও শূন্য। অর্থাৎ, Foxp3 যে Treg-এর নিয়ন্ত্রক তা বলতে বাধা রইল না।
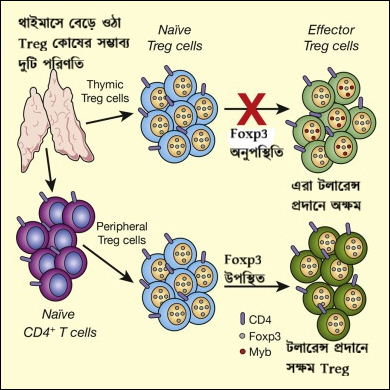
চিত্র-৫: কার্যকরী Treg তৈরি করতে FOXP3 প্রোটিনের উপস্থিতি একান্তই আবশ্যিক।
সুতরাং, এবারের নোবেলবিজয়ী বিজ্ঞানসন্দর্ভ প্রমাণ করে দিয়েছে যে ইঁদুরে এবং মানুষেও অটোইমিউন ডিজঅর্ডারের উৎস হল এক ধরণের টি-লিম্ফোসাইট সাবসেটের (Treg) অভাব এবং তাদের রেগুলেটর বা নিয়ন্ত্রক হিসাবে কাজ করা একটি স্বাভাবিক Foxp3 জীনের অনুপস্থিতি। স্বাভাবিক মানুষের স্বাভাবিক Foxp3 জীন সক্রিয় থাকলেই সে স্বাভাবিক ও সুস্থ। কিন্তু এই জীনের মধ্যে মাত্র একটি ক্ষুদ্রাতিক্ষুদ্র বদল যে বিকলনগুলো আনে তা হল যথাক্রমে Treg উৎপাদনে ব্যর্থতা, টি-লিম্ফোসাইটগুলোর অতিমাত্রায় সক্রিয়তা, নিজদেহের অঙ্গ-প্রত্যঙ্গ এইসব সক্রিয় টি-কোষের দাপটে ক্রমশ ঘায়েল হয়ে পড়া এবং বিভিন্ন অটোইমিউন ডিজঅর্ডারের লক্ষণগুলি প্রকট হওয়া, অবশেষে মৃত্যু। শরীরের স্থিতাবস্থার একটা লাতিন নাম রয়েছে - হোমিওস্ট্যাসিস। পল আর্লিচের 'হরর অটোটক্সিকাস' এই স্থিতাবস্থা বিপন্ন করা একটা পরিস্থিতি যার শিকার যতটা গবেষণাগারের ইঁদুর ঠিক ততোটাই মনুষ্যকূল। উভয়ের ক্ষেত্রেই পূর্বকথিত 'সেন্ট্রাল টলারেন্স'-এর রহস্য লুকিয়ে আছে Treg-এর কার্যকারিতার উপর এবং Treg কার্যকরী হবে কিনা তা নির্ভর করে Foxp3 (মানুষের ক্ষেত্রে এই জীনকে Caps-এ FOXP3 লেখার রীতি আছে) অবিকৃত কিনা তার ওপর। সুস্থভাবে বেঁচে থাকার জন্য মূল ইমিউনিটির অস্ত্রশস্ত্রর পাশাপাশি তাদের আত্মঘাতী আক্রমণ এড়িয়ে যাবার ক্ষমতাও থাকা দরকার। এটা ইমিউন সিস্টেমের একান্ত জরুরী একটি পার্শ্বীয় শাখা (Peripheral Immunity)।
এখনও চিকিৎসাক্ষেত্রে ইমিউনোজেনিক iTreg কোষ দ্বারা থেরাপির ব্যবহার ট্রায়াল স্তরে। বস্তুত iTreg কোষের বাণিজ্যিক উৎপাদনের সম্ভাবনাগুলি এখনও পরীক্ষার স্তরে রয়েছে। এর জন্য FOXP3-এর ওপর নির্ভরশীলতাকে অতিক্রম করার চেষ্টা চলছে। শিমোন সাকাগুচি সে কাজে সফলও হয়েছেন। এর গুরুত্ব অপরিসীম। জন্মগত অটোইমিউন রোগের হাত থেকে বাঁচা বা গর্ভে ভ্রূণ রিজেকশন বা প্রতিস্থাপিত অঙ্গের (যেমন কিডনি) রিজেকশন, টাইপ ওয়ান ডায়বেটিস, লুপাস এরিথাইমেটোসাস, মাল্টিপল স্ক্লেরোসিস ইত্যাদি হাজারো সম্ভাবনার কথা বলা যায় যার থেকে মুক্তি পাওয়া যেতে পারে। আবার ক্যান্সার চিকিৎসায় Treg-কে কিছুটা বিপরীতধর্মী কাজ করিয়ে ঘাতক টি-লিম্ফোসাইটগুলোকে যদি টিউমার কোষগুলোকে ধ্বংস করতে প্ররোচিত করা যায় তাহলে অনেক সম্ভাবনার দরজা খুলে যেতে পারে।
তথ্যসূত্রঃ
1. Hedestam, Gunilla Karlsson, Member of the Nobel Committee, and Kämpe, Olle, Chair of the Nobel Committee (2025). Immune tolerance The identification of regulatory T-cells and FOXP3. www.nobelprize.com
2. Brunkow, M. E., E. W. Jeffery, K. A. Hjerrild, B. Paeper, L. B. Clark, S. A. Yasayko, J. E. Wilkinson, D. Galas, S. F. Ziegler, and F. Ramsdell. 2001. 'Disruption of a new forkhead/winged-helix protein, scurfin, results in the fatal lymphoproliferative disorder of the scurfy mouse', Nat Genet, 27: 68-73.
3. Kappler, J. W., N. Roehm, and P. Marrack. 1987. 'T-cell tolerance by clonal elimination in the thymus', Cell, 49: 273-80.
4. Sakaguchi, S. 2000. 'Regulatory T-cells: key controllers of immunologic self-tolerance', Cell, 101: 455.

